4. 実験例
3Dマトリックス中の
単一細胞観察
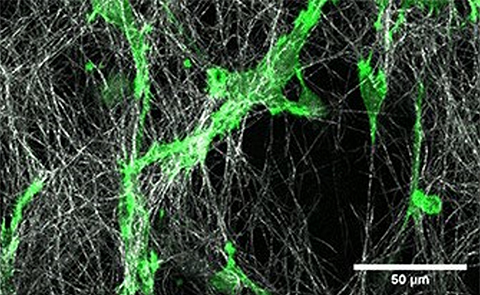
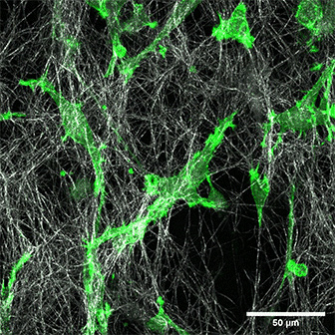
コラーゲンマトリックスでのHT‐1080癌細胞遊走3D生細胞イメージング
LifeActを発現するHT-1080細胞(緑色)を播種した マイクロスライド ケモタキシス上の1.5mg/mLI型コラーゲン(ラット尾由来)層(白色) 中に播種しました。 細胞遊走は、水浸対物レンズ40x/1.2を用いて、Zeiss共焦点顕微鏡LSM 880 AxioObserver上で300秒毎に撮影することにより記録しました。
スフェロイド培養、
オルガノイド培養
ウェブサイトで動画を見る方はこちらをクリック
特定のマイクロパターン上のスフェロイド形成
マイクロパターンは、3Dアッセイを最適化するための強力なツールである。ibidiのマルチセルアレイ用マイクロパターンスライドは、2Dおよび3D細胞培養している細胞の、特定の空間への配置を可能にするスライドである。細胞懸濁中の接着性細胞は、非接着性のBioinert表面には接着できず、接着パターン上にしか接着できないため、細胞は接着パターン上で凝集しスフェロイドを形成する。
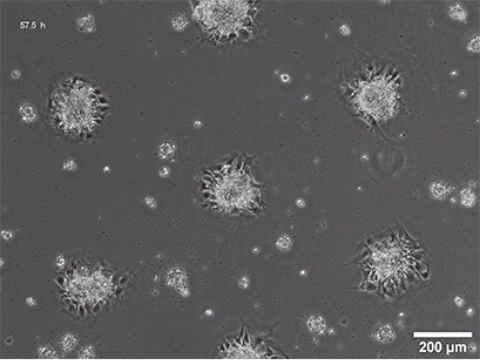
200 μmの接着斑上でのNIH‐3T3細胞(マウス胚線維芽細胞)のスフェロイド形成、スフェロイド生成が64時間立証された。位相差ライブセル撮像、4倍対物レンズ。
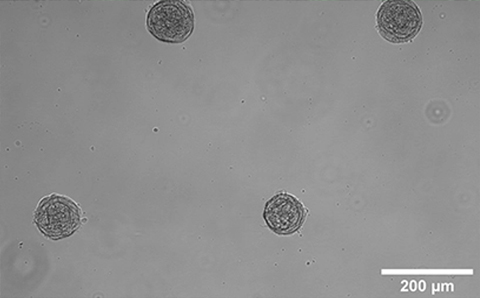
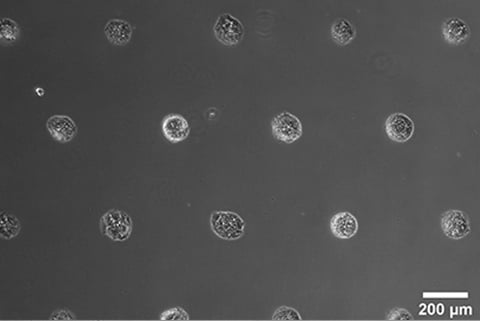
NIH-3T3細胞(マウス胚線維芽細胞)のスフェロイド形成。マルチセルアレイ用マイクロパターンスライドに細胞を播種してから14日後に撮影した。明視野顕微鏡使用。対物レンズ×10。
特定のパターンに沿って形成されたスフェロイド形成
NIH‐3T3細胞のスフェロイド形成。µ-Slide VI 0.4 With Multi-Cell µ-Pattern.に細胞を播種し、14日後の位相差顕微鏡に撮影。対物レンズ×4使用。
3Dコラーゲンゲル中の内皮細胞の出芽
浸潤性ヒト線維肉腫癌スフェロイド(HT‐1080)をI型コラーゲン(ラット尾由来)に埋めこんだ結果。マイクロスライド 8ウェルを使用し、ゲルマトリックスへの浸潤を48時間記録した。対物レンズ×4、明視野顕微鏡使用。
ウェブサイトで動画を見る方はこちらをクリック
ウェブサイトで動画を見る方はこちらをクリック
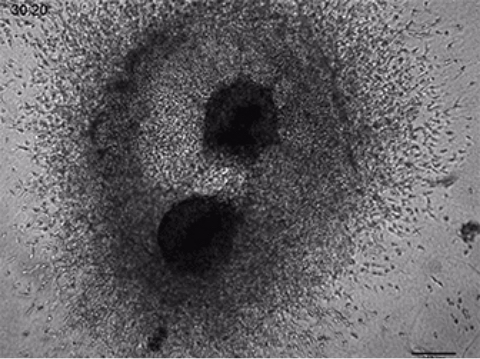
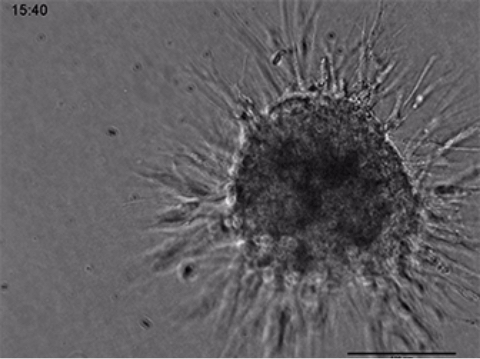
3Dコラーゲンゲル中の内皮細胞の出芽
I型コラーゲン(ラット尾由来)で作られた3Dゲルに埋め込まれたヒト臍帯静脈内皮細胞(HUVEC)のスフェロイドの生細胞イメージング。マイクロスライド 8ウェルを使用し、ゲルマトリックスへの出芽過程を44時間記録した。対物レンズ×10もしく×4、明視野顕微鏡使用。
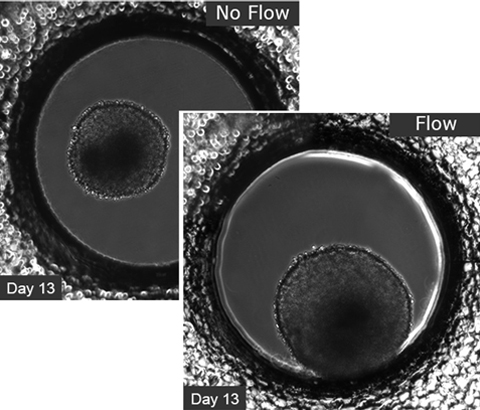
潅流培養でスフェロイドの成長が促進した事例
μL929線維芽細胞の マイクロスライド スフェロイド パフュージョン、Bioinertを用いたスフェロイド形成例。5 x105個/ mLで細胞を播種し、14日観察。
左:灌流なし 右:ibidiポンプシステムによる灌流、0.75mL /分。位相差顕微鏡、10倍の対物レンズ、ウェルの直径800 µm
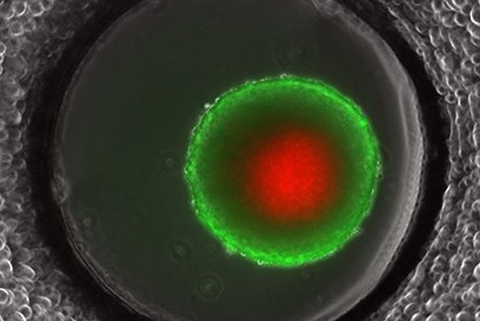
長期培養スフェロイドの生細胞、死細胞染色
ibidiポンプシステムとマイクロスライド スフェロイド パフュージョンを使用し、L929細胞スフェロイドを14日後培養し、FDA/PI染色を用いて生細胞、視細胞染色を行った。フロー速度は0.75 ml/min。緑色:生細胞(FDA);赤色:死細胞(PI)。広視野蛍光顕微鏡使用。対物レンズ×10。
3D走化性実験
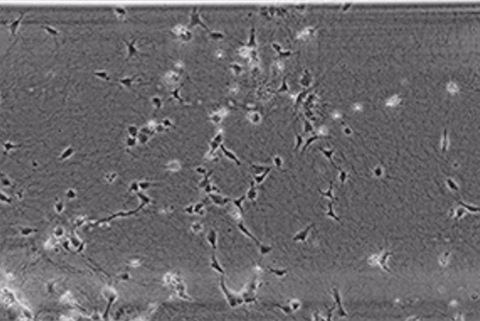
FCS勾配による3DコラーゲンIゲル中の内皮細胞の走化性
マイクロスライドケモタキシス上で、ヒト臍帯静脈内皮細胞(HUVEC)を1.5 μg/mlコラーゲンI型ゲルに包埋し、生細胞イメージングした結果。細胞は子牛胎児血清に向かって移動している。
位相差顕微鏡、対物レンズ×4、24時間の撮影
注意: 走化性の過程では、細胞同士が接触し、紐状になる場合があります。
ウェブサイトで動画を見る方はこちらをクリック